政策法規 || 《化學藥物殘留溶劑的風險評估和控制的共性問題(征求意見稿)》(附法規概覽1.19-1.23)
01
關于公開征求《化學藥物殘留溶劑的風險評估和控制的共性問題(征求意見稿)》意見的通知

點擊下方鏈接
查看詳細信息
https://www.cde.org.cn/main/news/viewInfoCommon/ac589f93f46056151fdf1b037788f4ad
02
關于公開征求ICH《E22:患者偏好研究的一般考慮》指導原則草案意見的通知

點擊下方鏈接
查看詳細信息
https://www.cde.org.cn/main/news/viewInfoCommon/9a9c3213a4f44e502bf7b18bbe93333d
03
關于公開征求《局部起效化學仿制藥物理化學及結構(Q3)特性研究技術指導原則(征求意見稿)》意見的通知

點擊下方鏈接
查看詳細信息
https://www.cde.org.cn/main/news/viewInfoCommon/38c7c506185f3f4090ff07f8934e835b
04
國家藥監局藥審中心關于發布《預防用疫苗佐劑藥學研究技術指導原則(試行)》的通告(2026年第7號)

點擊下方鏈接
查看詳細信息
https://www.cde.org.cn/main/news/viewInfoCommon/c21b81148b9b7908d172f97bf467d133
01
國家藥監局關于適用《Q8、Q9和Q10問答(R5)》國際人用藥品注冊技術協調會指導原則的公告(2026年第9號)

點擊下方鏈接
查看詳細信息
https://www.nmpa.gov.cn/xxgk/ggtg/ypggtg/ypqtggtg/20260119085720172.html
02
中藥保護品種公告(第34號)(2026年第11號)

點擊下方鏈接
查看詳細信息
https://www.nmpa.gov.cn/xxgk/ggtg/ypggtg/zhybhpzh/zhybhpzhgg/20260120085142173.html
03
國家藥監局關于45批次不符合規定化妝品的通告(2026年第2號)

點擊下方鏈接
查看詳細信息
https://www.nmpa.gov.cn/xxgk/ggtg/hzhpggtg/hzhpchjgg/hzhpcjgjj/20260120173328152.html
04
2026年1月23日中藥品種保護受理公示

點擊下方鏈接
查看詳細信息
https://www.nmpa.gov.cn/zwfw/zwfwgggs/zypzbhslgs/20260123143707128.html
01
國家藥監局藥審中心關于發布《藥物臨床試驗中應用貝葉斯外部信息借用方法的指導原則(試行)》的通告(2026年第6號)

點擊下方鏈接
查看詳細信息
https://www.cde.org.cn/main/news/viewInfoCommon/1b87c172f248c6eb876ea2b9d93c4d1e
02
關于將依維莫司微片納入《兒童抗腫瘤藥物研發鼓勵試點計劃(星光計劃)》試點項目的公示

點擊下方鏈接
查看詳細信息
https://www.cde.org.cn/main/news/viewInfoCommon/3c3ef49a5ab316a8d6ca95850b325dbb
03
關于將鹽酸匹米替尼膠囊納入《兒童抗腫瘤藥物研發鼓勵試點計劃(星光計劃)》試點項目的公示

點擊下方鏈接
查看詳細信息
https://www.cde.org.cn/main/news/viewInfoCommon/3dda22a2276c2601a3c797f7800ecf24
04
關于將ONC201膠囊納入《兒童抗腫瘤藥物研發鼓勵試點計劃(星光計劃)》試點項目的公示

點擊下方鏈接
查看詳細信息
https://www.cde.org.cn/main/news/viewInfoCommon/27cae5f5c6ee99cacdf0d86bc4bdb06b
01
近期,藥典委發布的標準草案公示如下:
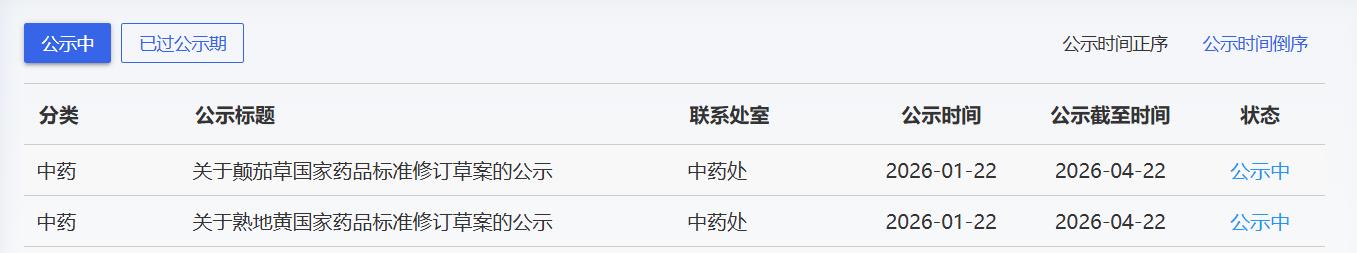
點擊下方鏈接
查看詳細信息
https://www.chp.org.cn/#/business/standard
-END-


轉載聲明:未經本網或本網權利人授權,不得轉載、摘編或利用其他方式使用上述作品。已經本網或本網權利人授權使用作品的,應在授權范圍內使用,并注明“來源:新領先醫藥科技”。

 Hotline服務熱線:010-83057670
Hotline服務熱線:010-83057670
 簡體中文
簡體中文

 010-83057670
010-83057670 聯系地址:
聯系地址: 技術市場部:
技術市場部: 北京新領先
北京新領先 新領先藥訊
新領先藥訊 010-61006450
010-61006450
